分享幣圈內容,享內容挖礦收益
placeholder
#VanEckCryptoETFJoins401kPlan
加密货币進入退休金融的聖殿
作者:Vortex_King
在金融演變的宏大編年史中,某些發展具有靜悄悄地重塑整個經濟范式的力量。它們可能不會以市場崩盤的雷鳴或投機泡沫的奇觀爆發,但其影響深遠到全球資本的未來。
這樣一種轉變最近從傳統退休規劃與數字資產創新的交匯處浮現。尊貴的資產管理機構VanEck已經開啟了一項非凡的舉措,現在允許精選的加密貨幣交易所交易基金在美國401k退休計劃中可用。
對於普通觀察者而言,這似乎只是另一項增量金融產品。然而,對於那些研究全球投資系統架構的人來說,它代表的東西遠為重要得多。
首次在有意義的規模上,數字資產開始滲透到長期退休資本的堡壘中。
因此,讓我們以謹慎的態度考察這一重大發展背後的力量、結構和影響。
401k系統的架構
在探討退休投資組合中加密貨幣交易所交易基金的意義之前,必須首先理解它們所進入的系統的規模。
美國401k退休框架構成了世界上最大的長期投資資本池之一。員工將其工資的一部分貢獻到稅收優惠賬戶,隨後這些資金被投資於各種多元化的金融工具中。
這些退休計劃統計起來代表著數萬億美元的資本,形成了全球投資生態系統的基石。
從歷史上看,此類計劃內的投資選擇一直故意保守。傳統配置通常包括股票、政府債券、公司債券和多元化指數基金。
投機性或波動性資產很少被允許在退休投資組合內。
因此,加
查看原文加密货币進入退休金融的聖殿
作者:Vortex_King
在金融演變的宏大編年史中,某些發展具有靜悄悄地重塑整個經濟范式的力量。它們可能不會以市場崩盤的雷鳴或投機泡沫的奇觀爆發,但其影響深遠到全球資本的未來。
這樣一種轉變最近從傳統退休規劃與數字資產創新的交匯處浮現。尊貴的資產管理機構VanEck已經開啟了一項非凡的舉措,現在允許精選的加密貨幣交易所交易基金在美國401k退休計劃中可用。
對於普通觀察者而言,這似乎只是另一項增量金融產品。然而,對於那些研究全球投資系統架構的人來說,它代表的東西遠為重要得多。
首次在有意義的規模上,數字資產開始滲透到長期退休資本的堡壘中。
因此,讓我們以謹慎的態度考察這一重大發展背後的力量、結構和影響。
401k系統的架構
在探討退休投資組合中加密貨幣交易所交易基金的意義之前,必須首先理解它們所進入的系統的規模。
美國401k退休框架構成了世界上最大的長期投資資本池之一。員工將其工資的一部分貢獻到稅收優惠賬戶,隨後這些資金被投資於各種多元化的金融工具中。
這些退休計劃統計起來代表著數萬億美元的資本,形成了全球投資生態系統的基石。
從歷史上看,此類計劃內的投資選擇一直故意保守。傳統配置通常包括股票、政府債券、公司債券和多元化指數基金。
投機性或波動性資產很少被允許在退休投資組合內。
因此,加


- 讚賞
- 1
- 1
- 轉發
- 分享
GateUser-95194dd2 :
:
細心觀察🔍LJz
陆家嘴
創建人@
上市進度
0.00%
市值:
$0.1
更多代幣
#财神每日币圈资讯
3月13日
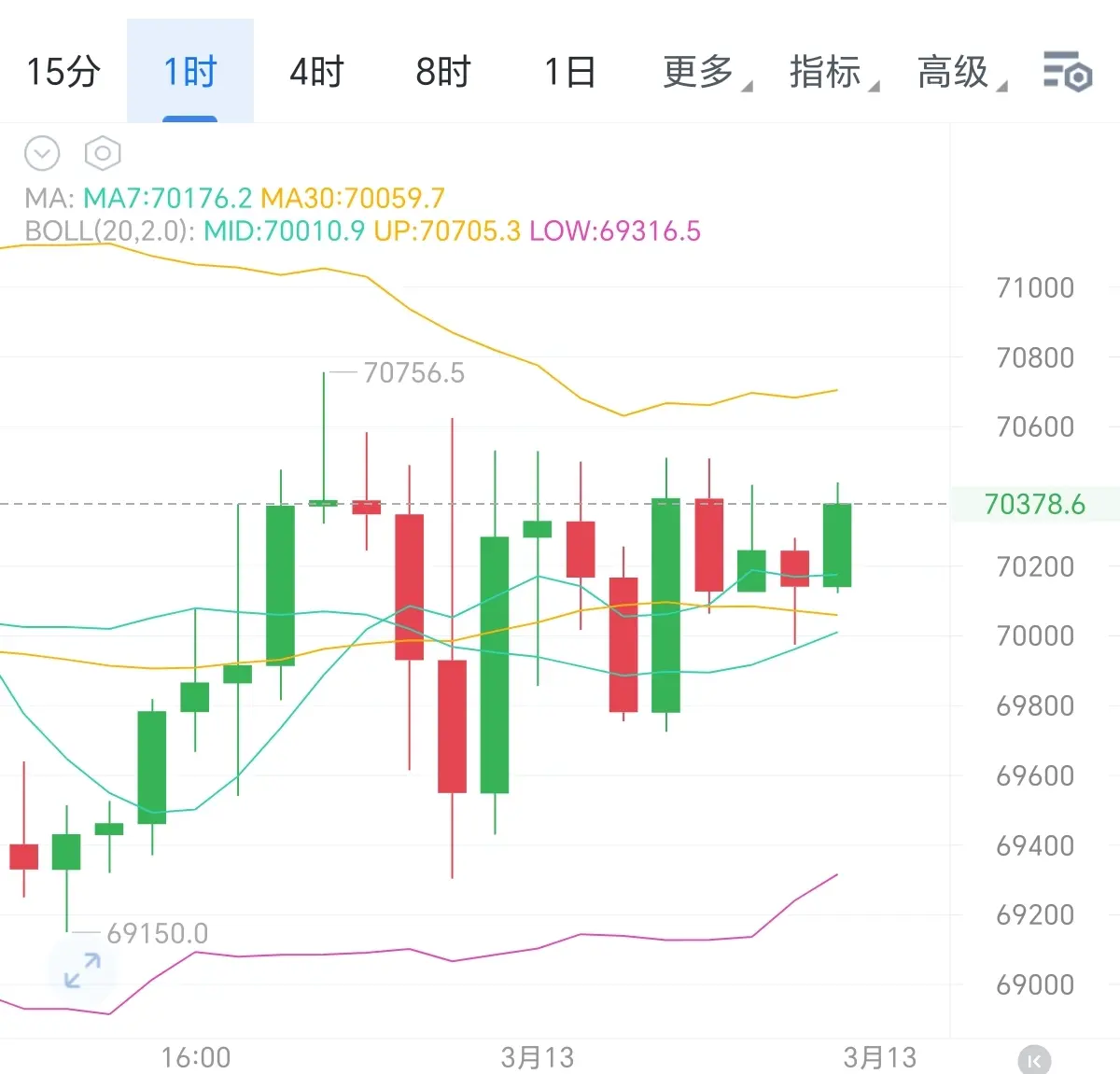
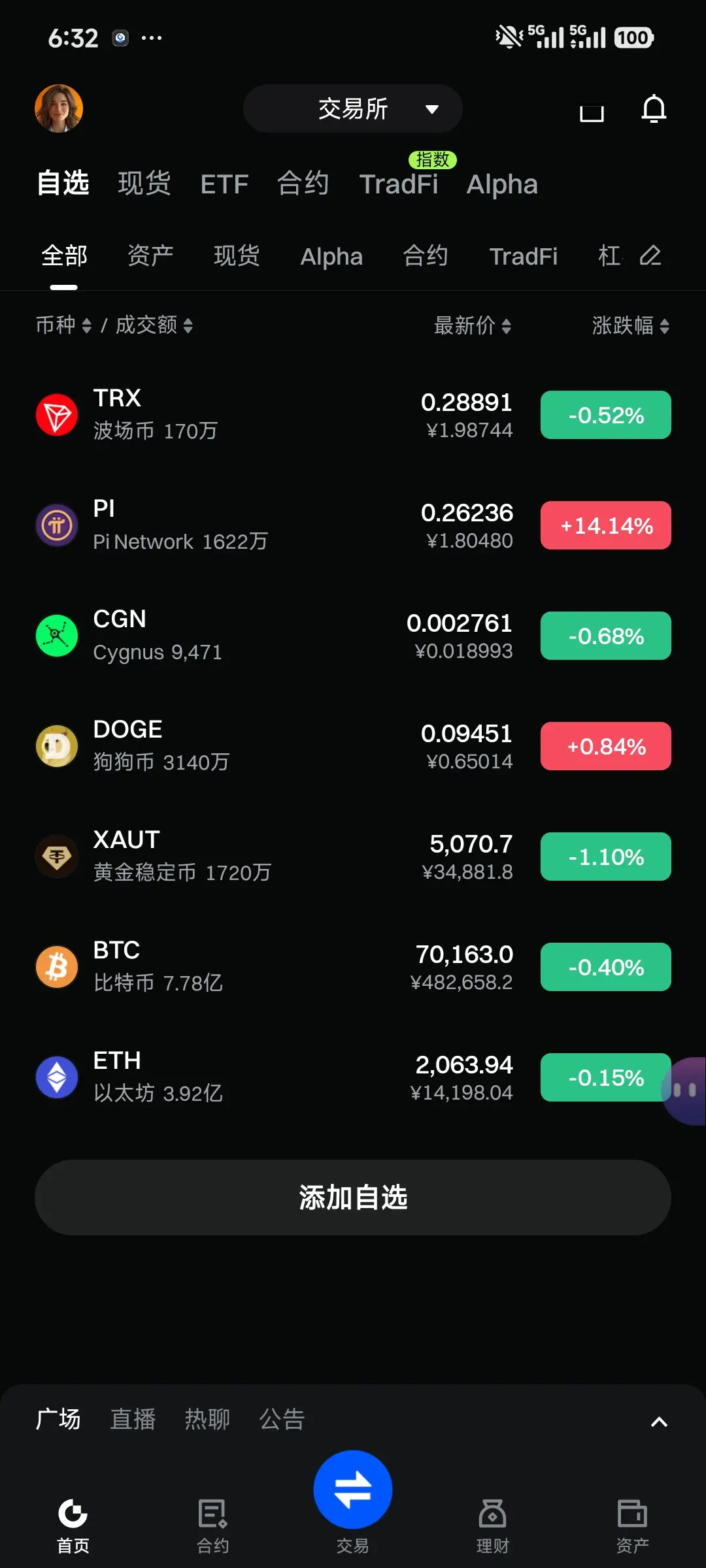
1.大饼行情:大饼高位震荡,最低报收69165,最高报收70758美元,现报收70500美元;以太走势强于大饼,最高报收2094美元,现报收2075.86美元
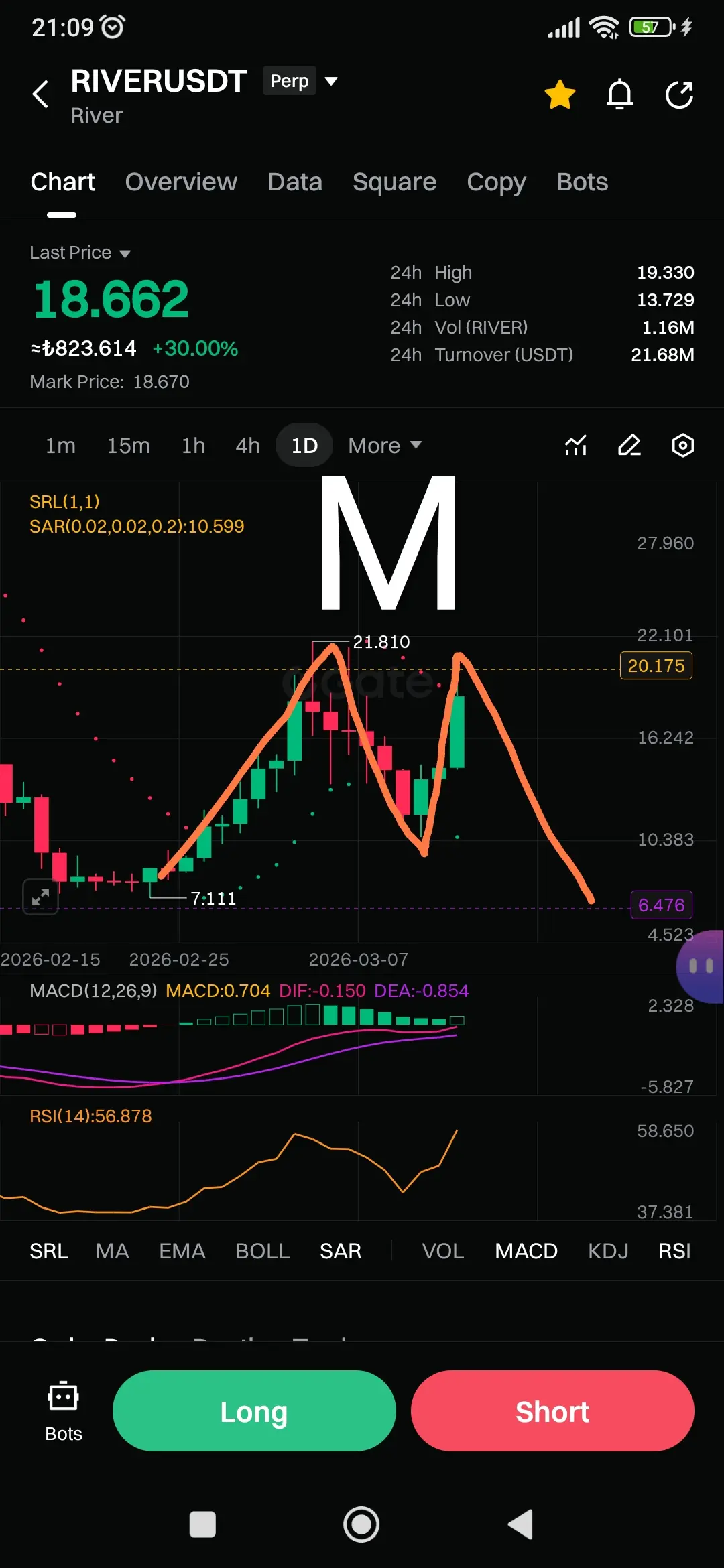
2.山寨市场:大饼震荡,山寨市场再次异彩纷呈,DOGE上涨2%,报收0.0947美元;LYN自低位反弹超过100%,报收0.3135美元;UAI强势上涨50%,报收0.33美元;TURBO上涨32%;RIVER上涨29%,报收18.8美元;PI上涨20%,报收0.27美元;PIXEL大跌27%,报收0.0106美元;中文meme"龍蝦"漲12%,報收0.0214美元
3.隔壁市場:美股三大指數集體收跌,納指跌1.78%,英特爾跌超5%,AMD、美光科技、特斯拉跌超3%;大A走出深V行情,創業板指跌1%;黃金跌2%,報收5084美元,白銀跌2%,報收85.95美元;國際原油大漲超10%,突破100美元大關,佈倫特原油報收101.59美元,美國WTI原油觸及96.39美元
4.時事要聞:伊朗新任最高領袖發表首次聲明,伊朗將繼續採取包括封鎖霍爾木茲海峽在內的戰略手段,同時對美國在中東地區的軍事基地發動攻擊。
5.時事要聞:伊朗副外長:允許部分國家船隻通過霍爾木茲海峽
6.財經資訊:美財長:美國財政部正提供一項臨時授權,允許各國購買目前滯留在海上的俄羅斯石油
7.幣圈新聞:CFTC發佈有關預測市場的
查看原文3月13日
1.大饼行情:大饼高位震荡,最低报收69165,最高报收70758美元,现报收70500美元;以太走势强于大饼,最高报收2094美元,现报收2075.86美元
2.山寨市场:大饼震荡,山寨市场再次异彩纷呈,DOGE上涨2%,报收0.0947美元;LYN自低位反弹超过100%,报收0.3135美元;UAI强势上涨50%,报收0.33美元;TURBO上涨32%;RIVER上涨29%,报收18.8美元;PI上涨20%,报收0.27美元;PIXEL大跌27%,报收0.0106美元;中文meme"龍蝦"漲12%,報收0.0214美元
3.隔壁市場:美股三大指數集體收跌,納指跌1.78%,英特爾跌超5%,AMD、美光科技、特斯拉跌超3%;大A走出深V行情,創業板指跌1%;黃金跌2%,報收5084美元,白銀跌2%,報收85.95美元;國際原油大漲超10%,突破100美元大關,佈倫特原油報收101.59美元,美國WTI原油觸及96.39美元
4.時事要聞:伊朗新任最高領袖發表首次聲明,伊朗將繼續採取包括封鎖霍爾木茲海峽在內的戰略手段,同時對美國在中東地區的軍事基地發動攻擊。
5.時事要聞:伊朗副外長:允許部分國家船隻通過霍爾木茲海峽
6.財經資訊:美財長:美國財政部正提供一項臨時授權,允許各國購買目前滯留在海上的俄羅斯石油
7.幣圈新聞:CFTC發佈有關預測市場的

- 讚賞
- 1
- 留言
- 轉發
- 分享
- 讚賞
- 按讚
- 1
- 轉發
- 分享
GateUser-b7ace3b3 :
:
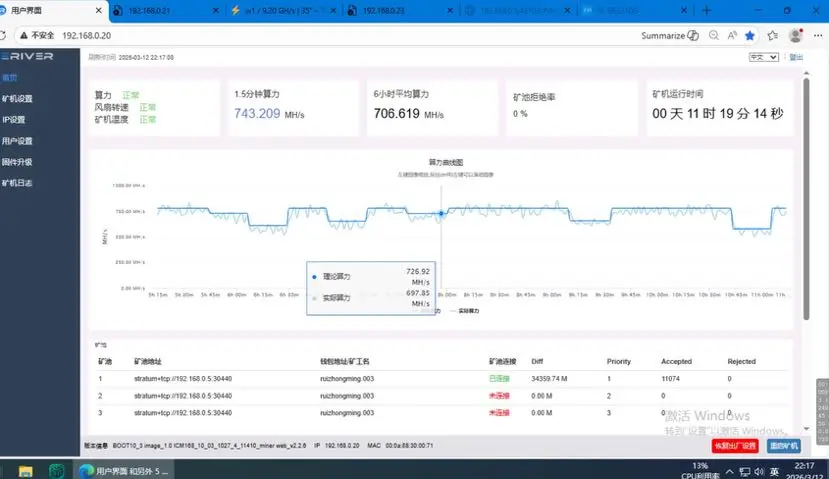
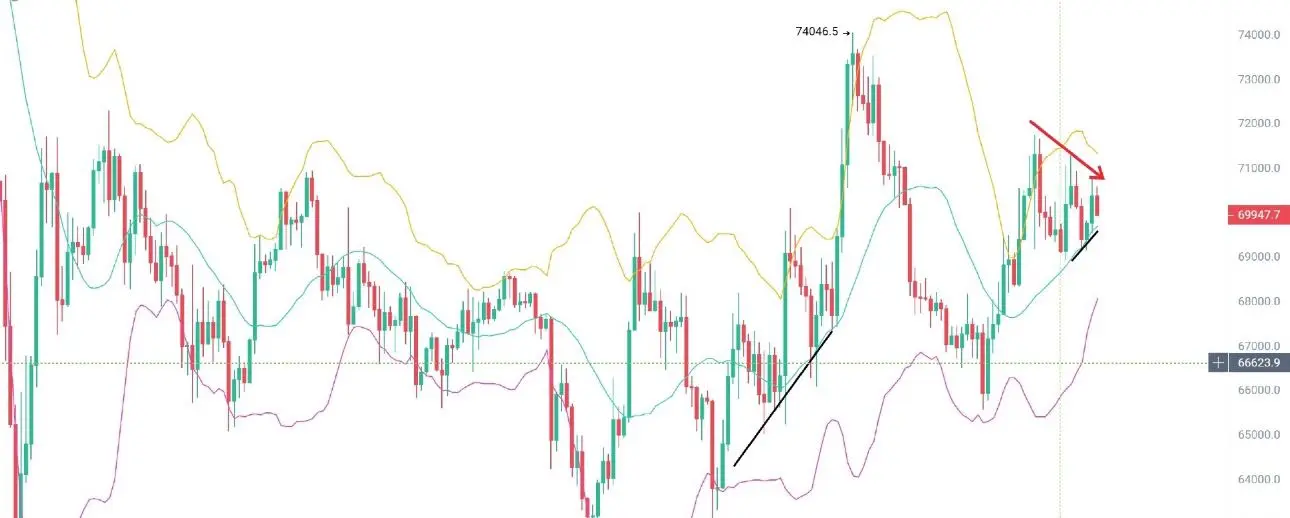
鱼池算力收益器570m一天收益5200個幣BTC從4小時指標和K線形態很有誘惑性看多
但日線和週線是不具備走上漲趨勢的
特別週線指標在這點卡了死死的
行情上方空間不大隨時會砸盤,
且主護盤還是以震盪微漲行為過度時間
最終還是要拋售砸盤的
以日線boll壓力位71800為頂
上方溢出點為8小時ema雙軌壓力72800
這也是3月4日高位74000的壓力線
目前71000附近為高位壓力點
行情最近回調都在69000點附近
昨日70200-71000高位空
今日上移70500-71300空
根據每天拉升的高位去空它
上方空間不大隨時要砸盤。
但日線和週線是不具備走上漲趨勢的
特別週線指標在這點卡了死死的
行情上方空間不大隨時會砸盤,
且主護盤還是以震盪微漲行為過度時間
最終還是要拋售砸盤的
以日線boll壓力位71800為頂
上方溢出點為8小時ema雙軌壓力72800
這也是3月4日高位74000的壓力線
目前71000附近為高位壓力點
行情最近回調都在69000點附近
昨日70200-71000高位空
今日上移70500-71300空
根據每天拉升的高位去空它
上方空間不大隨時要砸盤。
BTC0.46%
- 讚賞
- 3
- 3
- 轉發
- 分享
Kikikk :
:
原地空啊查看更多
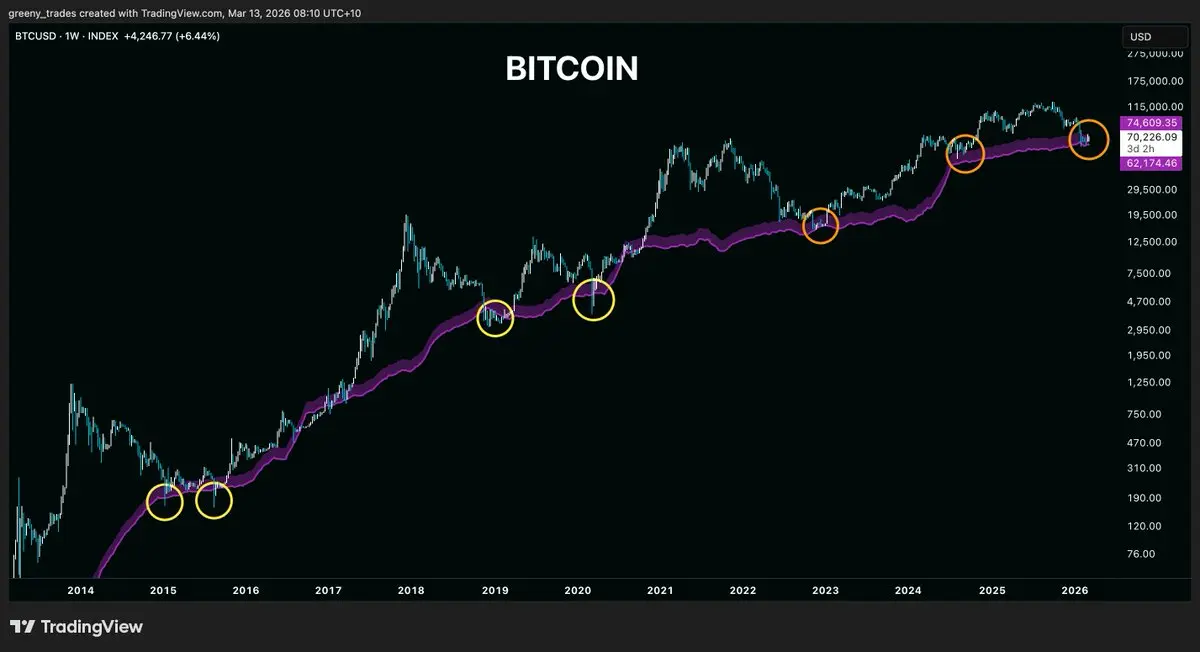
比特幣持平在70,000美元,卻沒人談論為什麼這個數字其實很恐怖。
生產成本區間目前位於62,000美元至70,000美元。這是礦工維持網絡運行的成本範圍。當價格跌入這個區間時,礦工們開始流血。當價格完全跌破這個範圍時,最弱的礦工會關閉機器並拋售他們擁有的一切。
這種被迫拋售才是創造真實底部的因素。
目前比特幣沒有接近這個區間。它正坐在這個區間內。礦工在這些價格下已經承受壓力,而市場卻表現得一切都很好。看看自2014年以來的每一次熊市,價格不僅觸及這個區間,還會突破它,製造恐慌,震出每一個弱手,然後強勁反彈。那些在礦工痛苦最大時買入的人獲得了改變人生的回報。
問題是,如果62,000美元被跌破且礦工投降發生時,你有計畫嗎?還是你只是希望低點已經出現?
生產成本區間目前位於62,000美元至70,000美元。這是礦工維持網絡運行的成本範圍。當價格跌入這個區間時,礦工們開始流血。當價格完全跌破這個範圍時,最弱的礦工會關閉機器並拋售他們擁有的一切。
這種被迫拋售才是創造真實底部的因素。
目前比特幣沒有接近這個區間。它正坐在這個區間內。礦工在這些價格下已經承受壓力,而市場卻表現得一切都很好。看看自2014年以來的每一次熊市,價格不僅觸及這個區間,還會突破它,製造恐慌,震出每一個弱手,然後強勁反彈。那些在礦工痛苦最大時買入的人獲得了改變人生的回報。
問題是,如果62,000美元被跌破且礦工投降發生時,你有計畫嗎?還是你只是希望低點已經出現?
BTC0.46%
- 讚賞
- 按讚
- 留言
- 轉發
- 分享
- 讚賞
- 按讚
- 留言
- 轉發
- 分享
- 讚賞
- 按讚
- 留言
- 轉發
- 分享
"曾经有一個時代,一段陷入困境的婚姻自動成為社區的責任。如果一個男人行為不當,他的兄弟們會被召來開導他。如果一個女人的態度不端正,她的家人會前去探訪,用愛心和堅定去糾正她。
每個人都明白,一個破碎的家庭可能會傷害許多未來的孩子,甚至影響村莊的名聲。現在人們說這是我的人生,誰都不能對我說三道四。那種自由聽起來很甜蜜,但結果卻是苦澀的。
孩子們在家庭之間流離失所,感到困惑和憤怒。祖父母與孫兒女失去聯繫。我們必須在現代權利和古老智慧之間找到平衡。當長者們以公正的心態介入時,他們仍然可以拯救許多婚姻免於以眼淚和警方報案而告終。" ~~Kanayo O. Kanayo
查看原文每個人都明白,一個破碎的家庭可能會傷害許多未來的孩子,甚至影響村莊的名聲。現在人們說這是我的人生,誰都不能對我說三道四。那種自由聽起來很甜蜜,但結果卻是苦澀的。
孩子們在家庭之間流離失所,感到困惑和憤怒。祖父母與孫兒女失去聯繫。我們必須在現代權利和古老智慧之間找到平衡。當長者們以公正的心態介入時,他們仍然可以拯救許多婚姻免於以眼淚和警方報案而告終。" ~~Kanayo O. Kanayo

- 讚賞
- 按讚
- 留言
- 轉發
- 分享
- 讚賞
- 按讚
- 留言
- 轉發
- 分享
OpenClaw
大龙虾
創建人@白羊吖丨
認購進度
0.00%
市值:
$0
更多代幣
- 讚賞
- 3
- 2
- 轉發
- 分享
GateUser-2216933f :
:
堅定HODL💎查看更多
我會繼續關注你,請不要覺得是命令
查看原文
- 讚賞
- 按讚
- 留言
- 轉發
- 分享
每個人都在交易相同的幣種。聰慧資金正在交易結果 💸⚡️💸
當零售交易者猛進迷因幣希望獲得 10 倍收益時,另一種類型的狂人卻在 Polymarket 上悄悄印鈔。Web3 最大的預測市場。
沒有雜音。只有信息市場,你的信念會得到回報。
📊 數字不會說謊:
• 每月 25 萬至 50 萬活躍交易者
• $18B 2025 年預計交易量
• 每月 1700 萬+ 網站訪問量
這不是一條鬼鏈。這是已經在運作的基礎設施。
🔌 設置只需 3 分鐘
連接 Phantom 或 MetaMask → 無需 KYC → 立即開始交易真實世界結果。USDC、ETH、加密貨幣或法幣 — 由你選擇。
當你等待下一個寶石飆升時,Polymarket 用戶已經在地緣政治、AI、體育、宏觀經濟等各自的專業領域內部創造收益。
🔥 背景很重要
→ $HYPE — 早期平台信徒獲得了巨大回報
→ $JTO (Jito) — 空投敘事推動了瘋狂的早期採用
⏳ Alpha 是敘事在進入你的時間線之前就誕生的地方。川普賠率、美聯儲決議、加密 ETF 批准 — 都在這裡先交易。
如果你一直是活躍用戶?圍繞 $POLY 的強大空投猜測正在累積。
Hyperliquid 的早期用戶沒有考慮兩次。Jito 的早期用戶也沒有。
你已經知道這個故事如何結束。
優勢不再僅存於圖表中。
而是在於關於接下來會發生什麼的正確判斷。
查看原文當零售交易者猛進迷因幣希望獲得 10 倍收益時,另一種類型的狂人卻在 Polymarket 上悄悄印鈔。Web3 最大的預測市場。
沒有雜音。只有信息市場,你的信念會得到回報。
📊 數字不會說謊:
• 每月 25 萬至 50 萬活躍交易者
• $18B 2025 年預計交易量
• 每月 1700 萬+ 網站訪問量
這不是一條鬼鏈。這是已經在運作的基礎設施。
🔌 設置只需 3 分鐘
連接 Phantom 或 MetaMask → 無需 KYC → 立即開始交易真實世界結果。USDC、ETH、加密貨幣或法幣 — 由你選擇。
當你等待下一個寶石飆升時,Polymarket 用戶已經在地緣政治、AI、體育、宏觀經濟等各自的專業領域內部創造收益。
🔥 背景很重要
→ $HYPE — 早期平台信徒獲得了巨大回報
→ $JTO (Jito) — 空投敘事推動了瘋狂的早期採用
⏳ Alpha 是敘事在進入你的時間線之前就誕生的地方。川普賠率、美聯儲決議、加密 ETF 批准 — 都在這裡先交易。
如果你一直是活躍用戶?圍繞 $POLY 的強大空投猜測正在累積。
Hyperliquid 的早期用戶沒有考慮兩次。Jito 的早期用戶也沒有。
你已經知道這個故事如何結束。
優勢不再僅存於圖表中。
而是在於關於接下來會發生什麼的正確判斷。
- 讚賞
- 按讚
- 留言
- 轉發
- 分享
- 讚賞
- 按讚
- 留言
- 轉發
- 分享
与我们分享,不要犹豫#GateAIGateClawOfficiallyLaunches
关于gete.io平台发展和人工智能的意见调查
查看原文关于gete.io平台发展和人工智能的意见调查

請把您想要翻譯的內容分享給我,我將會以完全誠實的方式提供意見並與您分享翻譯結果。
不過,我注意到您目前發送的是阿拉伯語文本,而我的專長是翻譯加密貨幣、Web3 和金融相關內容至繁體中文。
請提供:
- 需要翻譯的具體內容
- 來源語言確認
- 目標語言確認(應為繁體中文)
我會立即為您提供準確的翻譯。
成功且滿意
失敗且不滿意
0人參與還有22小時結束
- 讚賞
- 按讚
- 留言
- 轉發
- 分享
加載更多
加入 4000萬 人匯聚的頭部社群
⚡️ 與 4000萬 人一起參與加密貨幣熱潮討論
💬 與喜愛的頭部創作者互動
👍 查看感興趣的內容
熱門話題
查看更多11.68萬 熱度
4.49萬 熱度
13.22萬 熱度
14.61萬 熱度
174.04萬 熱度
熱門 Gate Fun
查看更多- 市值:$2420.68持有人數:10.00%
- 市值:$0.1持有人數:10.00%
- 市值:$0.1持有人數:00.00%
- 市值:$2417.24持有人數:10.00%
- 市值:$0.1持有人數:00.00%
最新消息
查看更多今日加密貨幣恐慌與貪婪指數跌至 15,市場仍處極度恐慌狀態
5 分鐘前
ETH 15-minute rise of 0.79%: Liquidity's staged decline and short-term capital arbitrage resonance drive uptrend
5 分鐘前
BTC 15分钟上涨0.84%:鏈上資金流動與技術面突破共振推動異動
5 分鐘前
Meta 新 AI 模型因性能未達預期推遲發布,代號 Avocado
5 分鐘前
CME "Fed Watch": Probability of Maintaining Interest Rates Unchanged in March at 99.1%
6 分鐘前
置頂
Gate Booster 第 4 期:發帖瓜分 1,500 $USDT
🔹 發布 TradFi 黃金福袋原創內容,可得 15 $USDT,名額有限先到先得
🔹 本期支持 X、YouTube 發布原創內容
🔹 無需複雜操作,流程清晰透明
🔹 流程:申請成為 Booster → 領取任務 → 發布原創內容 → 回鏈登記 → 等待審核及發獎
📅 任務截止時間:03月20日16:00(UTC+8)
立即領取任務:https://www.gate.com/booster/10028?pid=allPort&ch=KTag1BmC
更多詳情:https://www.gate.com/announcements/article/50203🤖 尋找 Gate 廣場 AI 評測官!$50,000 懸賞令發布!
發帖聊 AI,獎金拿到手軟!新人首帖獎勵翻倍,單帖最高 200U!
📝 立即報名:https://www.gate.com/questionnaire/7477
1️⃣ 發帖得紅包,單帖最高 100U!
2️⃣ Top 體驗分享官:帶 #Gate广场AI测评官 聊技巧,贏國米球衣!
3️⃣ 收益率 PK 王:曬 AI 收益截圖,贏 Gate 定制運動套裝!
4️⃣ 深度好文額外加碼 30U 每篇張榜公布!
💬 來 Gate 廣場,把握行業新趨勢:https://www.gate.com/post
時間:3/12 18:00 – 3/27 24:00 (UTC+8)
詳情:https://www.gate.com/announcements/article/50206Gate 廣場|3/12 今日熱議: #原油价格上涨
🎁 帶話題或 BTC 幣對發帖,抽 5 位錦鯉送出 $2,500 仓位體驗券!
中東局勢突變:阿曼原油出口碼頭全面疏散,伊拉克石油港口停運,兩艘油輪在海灣遇襲,原油供應警報拉滿!國際能源署釋放4億桶儲備,多空對決進入白熱化。
💬 本期熱議
1️⃣ 外交局勢:伊朗開出停戰條件,美伊能否達成共識?
2️⃣ 石油博弈:你看好誰?預測下一步油價走勢。
3️⃣ 加密走勢:油價資金流向將如何影響加密市場?分享你的分析。
立刻分享觀點 👉 https://www.gate.com/post
Gate TradFi,一鍵捕捉原油機遇 👉 https://www.gate.com/tradfi
📅 3/12 15:00 - 3/14 18:00 (UTC+8)Gate 廣場內容挖礦獎勵繼續升級!無論您是創作者還是用戶,挖礦新人還是頭部作者都能贏取好禮獲得大獎。現在就進入廣場探索吧!
創作者享受最高60%創作返佣
創作者獎勵加碼1500USDT:更多新人作者能瓜分獎池!
觀眾點擊交易組件交易贏大禮!最高50GT等新春壕禮等你拿!
詳情:https://www.gate.com/announcements/article/49802